본문
생명과학의 최전선, 1밀리미터 인간: 예쁜꼬마선충
이준호 교수(서울대학교 생명과학부)

1. 예쁜꼬마선충, 너는 누구냐?
2024년 10월 첫째 주 월요일인 7일 저녁, 반가운 소식이 전해졌다. 예쁜꼬마선충 연구자 두 사람이 노벨생리의학상을 수상했다는 것이었다. 빅터 앰브로스 교수와 개리 루브칸 교수가 영광의 주인공이었다. 그런데 예쁜꼬마선충 연구자가 노벨상을 받은 것이 이때가 처음이 아니다. 무려 4번의 노벨상이 예쁜꼬마선충에 주어졌다. 눈에 보이지도 않는 작은 선충이 그렇게 유명한 동물이었던가? 예쁜꼬마선충의 어떤 점이 연구자와 노벨상 위원회의 마음을 사로잡은 것일까?
2. 예쁜꼬마선충을 생물학 무대에 데뷔시킨 과학자

1963년 어느 날 시드니 브레너 박사는 자신의 연구소의 소장인 막스 페루츠 박사에게 연구비를 요청하는 장문의 편지를 쓰는데, 그 편지가 예쁜꼬마선충을 생물학의 무대에 데뷔시킨 사건이었다. 브레너 박사는 페루츠 소장에게 보낸 이 유명한 편지에서 분자생물학의 미래는 발생과 신경계 연구에 달려 있다고 주장하면서 미생물처럼 단순한 동물에 대한 연구가 중요하고, 그 목적에 잘 맞는 예쁜꼬마선충을 연구하는 것이 필요하다고 주장하였다. 1963년이 어떤 때인가를 살펴보면 브레너 박사가 얼마나 선구자적 안목을 가진 분인지 알 수 있다. 유전물질인 DNA의 구조가 이중나선으로 되어 있음을 주장하는 논문이 1953년에 발표됨으로써 현대적 의미의 분자생물학이 시작되었다고 본다면, 1963년은 분자생물학이 시작된 지 불과 10년이 지났을 뿐인 여명기였다. 다른 사람들이 DNA, RNA, 단백질 등 분자생물학의 중심 물질들에 집중하고 있을 때 브레너 박사는 그 훨씬 너머의 세계를 상상하고 있었던 것이다. 발생이란 정자와 난자가 만나 하나의 수정란을 만들고 그 수정란이 분열과 분화를 거듭하여 하나의 온전한 동물 개체를 만들어 가는 과정이라고 요약할 수 있다. 인간의 원초적 호기심의 대상 중 하나는 발생이라는 생명현상이 차지하고 있으니 생명과학의 원대한 목표가 틀림없다. 신경계란 다른 말로는 뇌라고 할 수 있겠다. 인간의 뇌는 작은 우주라고 할 만큼 복잡하고 신비한 생명현상의 집약체이다. 인간의 뇌를 이해하기 위해서는 정말 단순한 동물의 뇌부터 이해하는 것이 중요하다고 생각하는 것이 상식적이고 논리적인 방식이다. 발생과 신경계 연구를 위해 예쁜꼬마선충은 우리에게 주어진 선물과 같은 존재이다. 그런데 막상 브레너 경은 예쁜꼬마선충에 대해 처음부터 전문가는 아니었다. 그 반대였다. 미국의 UC 버컬리 대학의 도허티 교수에게 예쁜꼬마선충 분양을 부탁하는 편지가 지금도 남아 있는데 거기에 브레너 경의 상황이 고스란히 드러나 있다(그림2).
3. 시드니 브레너 경의 원대한 목표 1: 발생
브레너 경이 예쁜꼬마선충을 대상으로 발생과 신경계 연구를 할 수 있을 것이라고 생각한 이유가 당연히 있을 것이다. 그 중 가장 중요한 것은 예쁜꼬마선충은 다른 복잡한 구조의 동물과는 달리 단순한 형태를 가진 동물이면서도 발생과 신경계를 다 보유하고 있다는 점이었다. 당시 분자생물학 연구를 하기 위한 대상으로는 세균이나 세균을 감염시키는 바이러스(박테리오파지라고 부른다)가 주를 이루고 있었는데 세균이나 바이러스는 발생이나 신경계를 가지고 있지 않으니 아예 연구 대상이 될 수 없었다. 당시 가장 보편적인 동물 모델로 초파리가 있었고 지금도 가장 좋은 동물 모델 중 하나로 쓰이고 있지만 당시에는 너무나 복잡한 발생과정과 신경계를 가지고 있어서 발생과 신경계 연구를 하기 힘들었다. 브레너 경이 '미생물’과 비슷한 수준의 단순성을 가지는 예쁜꼬마선충을 선택한 것은 어찌 보면 과학의 역사에 있어 필연적인 과정이라 볼 수 있다.
브레너 경의 예쁜꼬마선충 연구 계획은 참으로 무모할 정도로 방대하고 원대한 것이었다. 우선 발생 연구를 위해서 브레너 경은 예쁜꼬마선충의 정상적인 발생과정을 샅샅이 알아내야 한다고 생각하였다. 그래서 수정란에서부터 성체에 이르기까지의 모든 발생 과정에서의 세포분열과 분화의 결과를 기록해서 족보를 만들 수 있다면 어느 계보에서 문제가 생긴 돌연변이를 찾아내어 각각의 발생 과정의 기전을 밝힐 수 있을 것이라고 생각하였다. 그래서 만들게 된 것이 세포계보(cell lineage)이다. 존 설스턴 박사가 브레너 박사 연구실의 박사후연구원으로 한 일이 매일 현미경을 보고 세포분열을 관찰하고 기록하는 일이었다. 그 일을 3년간 계속하여 논문 한 편을 썼고 다시 3년을 더하여 두 번째 논문을 쓰게 되었다. 이 두 편의 논문을 합치면 수정란에서부터 성체에 이르기까지의 모든 세포분열에 대한 완성된 계보가 되었고, 예쁜꼬마선충의 모든 세포들은 이름을 가지게 되었다. 이름을 가지게 되었다는 것은 그 운명 또한 정확히 알려졌음을 의미한다(그림3).
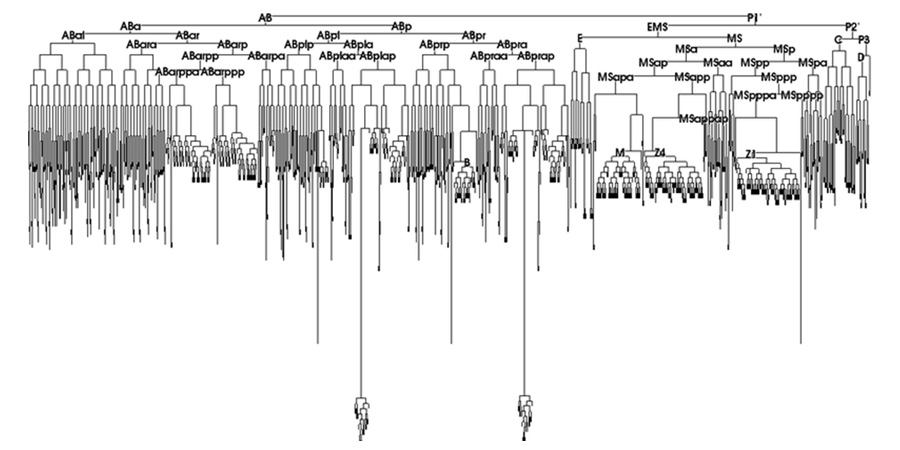
브레너 경의 연구실에서는 본격적으로 세포계보에 문제가 생기는 돌연변이를 찾아가는 일을 하게 된다. 예쁜꼬마선충을 연구한다고 할 때 대부분의 경우는 유전학 연구를 하는 것이고, 유전학 연구란 돌연변이를 연구하여 정상적인 유전자의 기능을 유추하고 확인하는 과정이라고 요약할 수 있다. 이렇게 대대적으로 찾아낸 돌연변이들에 대응하는 유전자들의 이름에 lin-이 붙어 있는 경우는 그 유전자에 돌연변이가 생기면 특정 세포계보에 문제가 생기는 표현형질을 나타낸다는 의미를 내포하고 있다. 예를 들면 lin-1은 세포계보가 잘못된 최초의 돌연변이고 lin-2는 두 번째, lin-3은 세 번째 돌연변이인 것이다. 수많은 lin- 돌연변이들이 동정되었고, 각 돌연변이가 일어난 유전자를 찾아 가는 일이 예쁜꼬마선충을 이용한 발생 유전학의 전형적인 방법이 되었다. 이런 식으로 찾아낸 돌연변이 중에 lin-4도 있었고, lin-14도 있었는데 이 두 유전자는 2024년 노벨 생리의학상의 소재가 되었으니 브레너 경의 원대한 계획이 수십년이 지난 후 현실에서 빛을 발하는 것임을 우리는 즐거운 마음으로 목격하였다.
4. 시드니 브레너 경의 원대한 목표 2: 신경계
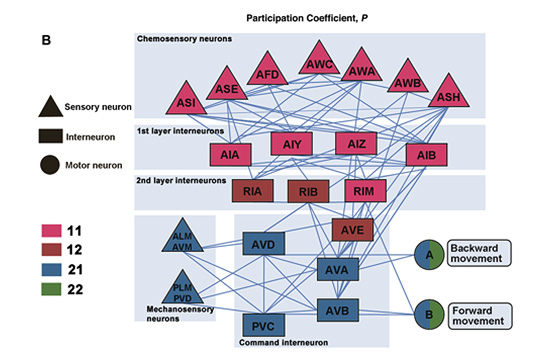
브레너 경의 두 번째 원대한 계획은 신경계에 관한 것이었다. 신경계를 이해한다는 것은 신경계가 어떻게 생겼고 어떻게 기능하는가를 세포 수준을 넘어 시냅스의 수준에서부터 회로의 수준에 이르기까지 총체적으로 이해하는 것이라고 할 수 있다. 이 정도로 신경계를 이해하려면 일단은 단순할수록 좋을 것이다. 예쁜꼬마선충은 302개의 뉴런으로 신경계를 이루고 있으니 이보다 단순한 신경계는 자연에서 찾기 힘들 것이다. 브레너 경은 이 단순한 신경계를 샅샅이 알고 연구를 시작하기로 마음을 먹었다. 그래서 브레너경의 후예들이 1970-80년대에 한 일은 지금 보아도 비현실적으로 보일 정도로 무모한 것이었다. 세포계보를 다 알겠다고 생각한 것과 견주어도 전혀 밀리지 않는 무모한 도전. 바로 전자현미경의 해상도로 신경계 전체를 재구성하겠다는 것이었다. 실제로 성체 한 마리를 50나노미터 두께로 잘라서 연쇄절편을 만들고 모든 절편에 대해 전자현미경 이미지를 찍어냈다. 그리고는 각 절편에 드러나는 모든 신경세포들의 모양을 추적하여 전체 신경계의 모양을 재구성하였다. 더욱 놀라운 일은 각 절편의 이미지를 샅샅이 뒤져서 모든 시냅스 즉 신경과 신경이 만나는 교통의 지점을 포착해 냈다는 것이다. 시냅스는 화학 시냅스와 전기 시냅스로 나눌 수 있는데 이 두 종류의 시냅스는 그 모양이 각각 독특하여 숙련된 전문가들이 잘 관찰하면 크게 실수하지 않는 선에서 시냅스를 찾을 수 있었다. 물론 엄청난 노동과 시간을 썼다. 그 결과는 참으로 대단하였다. 신경계의 모든 연결망이 모두 알려진 유일한 동물! 세포계보가 알려진 유일한 동물인 것만 해도 대단한데 신경계의 모든 연결을 지도로 만들었다니 놀랍지 않은가. 이 지도를 바탕으로 어떤 연결이 어떤 기능을 하는가를 찾아가는 연구의 기반이 될 수 있었던 것인데 그런 연구는 이 뇌지도가 완성된 후 30년 정도를 기다려야 했다(예를 들어 그림 4 참조). 그 정도로 선구적인 연구였다. 지금은 모든 신경계의 연결의 총합을 커넥톰(connectome)이라고 부르지만 예쁜꼬마선충의 신경계가 모두 밝혀지는 때에는 이런 이름 조차도 없었다.
5. 예쁜꼬마선충과 노벨상
본격적으로 예쁜꼬마선충 연구로 노벨상에 이르게 된 연구 업적들을 살펴보자. 첫 노벨상은 2002년에 나왔는데 시드니 브레너 경과 그의 제자 로버트 호르비츠 교수와 존 설스턴 교수 등 3인이 공동수상하였다. 일반적으로 노벨상 위원회는 수상자를 발표하면서 그 업적을 한 줄로 요약 정리해서 발표하는데, 2002년 노벨 생리의학상에 이르게 된 업적은 기관의 발생과 프로그램되어 있는 세포사멸의 조절에 대한 규명이었다. 기관의 발생이란 사실 발생학 전분야를 이르는 말일 수도 있을 만큼 광범위한 의미를 가지는 용어임에도 굳이 사용한 것은 시드니 브레너 경의 원대한 예쁜꼬마선충 연구에 대한 인정의 의미를 가지고 있었다고 생각하게 된다. 2002년 노벨 생리의학상의 구체적인 업적은 세포사멸, 그것도 단순한 세포사멸이 아니라 프로그램되어 있는 세포사멸이라는 생명현상의 발견이었다. 노벨 생리의학상은 노벨의 유언에 의해 가장 중요한 발견을 한 학자에게 수여되는 상이다. 중요한 다른 조건 하나는 인류에 기여할 수 있는 발견이어야 한다는 점이다. 예쁜꼬마선충 연구로 어떻게 인류에 기여할 수 있다는 말인가? 프로그램된 세포사멸 현상이 선충에서만 일어나는 현상이 아니고 진화적으로 잘 보존된 현상일 뿐 아니라 그 과정에 관여하는 유전자들이 사람에서도 존재하고 비슷한 일을 한다면 이야기는 달라진다. 예쁜꼬마선충에서의 대단한 발견이 인류에 기여할 수 있게 되는 것이므로 노벨 생리 의학상의 당당한 대상이 될 수 있는 것이다. 실제로 프로그램된 세포사멸에 관여하는 유전자들이 사람을 포함한 다른 동물에서도 잘 보존되어 있음이 밝혀졌다.
최초의 발견이 항상 어려운 일이다. 그럼 어떻게 예쁜꼬마선충에서는 세포사멸이 프로그램되어 일어난다는 것을 알아낼 수 있었을까? 그림 5에 그 해답이 있다. 세포계보의 일부를 확대한 이 그림을 잘 보면, 세포분열 후 만들어지는 세포 중 어떤 세포는 X로 표시되어 있음을 볼 수 있다. 바로 죽어 나간 세포를 의미한다. 다른 표현으로는 X표를 당한 세포는 언제나 그 자리에서 죽는다, 즉 저 세포들은 태어나서 하는 일은 죽는 일 밖에 없다. 개체에 관계없이 동일한 계보를 타고 만들어지는 세포 중 죽어나가는 세포는 전혀 다르지 않고 일정하다. 이런 일이 131군데에 일어나는데, 프로그램되어 있음을 가정하지 않으면 설명할 방법이 없는 현상이다. 프로그램은 당연히 유전자에 되어 있을 것이고, 유전자의 변이에 의해 세포사멸 양상이 달라질 것이므로 돌연변이를 찾아서 세포사멸 기전을 밝힐 수 있게 된 것이다. 그 후 그 유전자들의 분자 수준에서의 규명을 통해 진화적으로 보존된 세포사멸현상을 이해할 수 있게 되었고, 질병의 치료에 응용할 수 있게 되었으니, 노벨상 감이 아닐 수 없다.
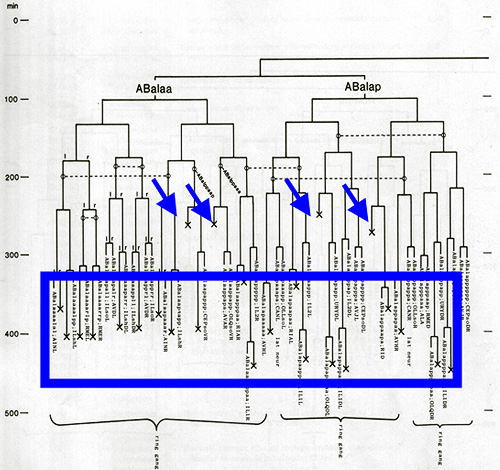
두 번째 노벨상은 RNA 간섭현상의 발견에 주어졌다. 앤디파이어와 크레이그 멜로 교수는 각각 다른 발생 연구를 하고 있었는데, 공통의 관심사는 antisense RNA 방법이 왜 항상 작동하는 것은 아닌지 하는 것이었다. antisense RNA 방법이란, 제어하고 싶은 유전자에서 만들어지는 mRNA와 상보적으로 결합할 수 있는(그래서 antisense라고 부른다. 정방향을 sense라고 부르므로 그 반대가 antisense가 되는 것이다) antisense RNA를 만들어 넣어주면 수소결합을 해서 단백질 합성을 위한 리보좀 결합을 방해함으로써 유전자 발현을 낮출 수 있을 것이라는 접근방법이다. 그런데 이론적으로는 그럴듯하지만 이 방법은 될 때도 있지만 작동하지 않을 때도 많았다. 그래서 위 두 교수는 sense RNA, antisense RNA, 그리고 이 둘을 섞은 RNA(아마도 double strand RNA로 되어 있을 것이다)를 정교하게 순수 분리를 해서 실제로 어떤 RNA가 단백질 합성을 저해하는지를 조사하였다. 그 결과는 놀라운 것이었는데 antisense RNA가 잘 작동하리라는 기대와는 달리 이중 가닥 RNA가 예상되는 역할을 유일하게 수행하는 것이었다! 특정 유전자의 기능을 낮추고자 할 때 이제는 RNA 간섭현상을 이용한 방법이 모든 생물에 적용되고 있고 발암유전자 발현을 억제하는 신약 개발의 표적이 되기도 하니 중요한 발견에 인류에 기여라는 조건을 충족시킨다고 할 수 있겠다.
노벨상 세 번째는 참 특이하다. 생리의학상이 아니라 화학상이다. 마틴 찰피 교수가 그 주인공인데, 살아있는 개체에서 원하는 단백질에 형광을 내도록 만들어서 그 단백질 발현의 정확한 시간과 장소를 찾아가는데 결정적인 기여를 한 녹생형광단백질 유전자의 효능을 최초로 증명해 보였다는 점에서 노벨 위원회가 인정한 것이다. 여기서 주목할 만한 점은 노벨이 유언에서 화학상의 경우 가장 중요한 발견 또는 개선을 이룬 학자에게 수여하라고 정해 두었다는 점이다. 녹색형광단백질의 발견에만 의미 부여를 했다면 그 유전자를 발견한 다른 두 명의 수상자만 수상 자격 해당이 되었을 것인데 개선, 즉 새로운 역할을 규명하는 일도 인정을 할 수 있었기 때문에 찰피 교수가 화학상을 받을 수 있었던 것이다.
가장 최근의 예쁜꼬마선충 노벨상은 2024년에 나왔는데 마이크로RNA 연구를 한 빅터 앰브로스 교수와 개리 루브칸 교수가 수상하였다. 이들은 각각 lin-4, lin-14 유전자를 연구하였는데 이들 유전자에 변이가 생기면 발생의 특정 단계를 반복하거나 생략하는 표현형질을 나타내는 것을 보고 발생의 시간이 프로그램되어 있다는 점을 간파하였고 그 기전을 극적으로 증명하였다. lin-4는 단백질 정보를 가지지 않은 엉뚱한 구조의 유전자였고 RNA까지만 만들어짐이 밝혀졌다. 그런데 이 RNA는 lin-14의 mRNA에 결합할 수 있어서 lin-14의 기능을 억제하는 방향으로 작용할 수 있음이 밝혀졌다. 이런 종류의 RNA를 마이크로RNA라고 명명하고는 더 나아가 다양한 생물들에서 비슷한 형태의 RNA 유전자가 존재함을 밝혔다. 마이크로 RNA의 이상이 인간 질병의 원인으로 조사되는 등 사람에 적용되는 사례가 늘어나고 있었으니 중요한 새로운 발견과 인류에의 기여라는 두 가지 조건을 아주 잘 만족한 사례로 볼 수 있다.
6. 우리의 연구 그리고 미래
예쁜꼬마선충 연구자들이 4번이나 노벨상을 받을 때 우리나라 연구자들을 뭐하고 있었을까? 노벨상의 역사를 자세히 들여다보면 수상 대상이 되는 연구 업적은 완성된 후 평균적으로 20-30년 정도의 시간이 필요했음을 알 수 있다. 우리나라의 20년 전은 어땠을까? 우리나라에서 본격적으로 예쁜꼬마선충 연구가 시작된 것은 1995년 경이다. 즉 20년 전에 우리나라는 예쁜꼬마선충 연구를 시작했을 뿐이니 당장 노벨상을 기대하는 것은 너무 이르다. 다만 지난 20년 동안 나름 중요한 연구 업적들이 축적되어 온 것은 사실이다. 필자의 연구실에서 진행된 연구 두 가지만 소개하고 본 글을 끝내고자 한다. 그 중 첫 번째 연구는 히치하이킹 행동에 관한 연구이다. 이 연구의 시작점은 닉테이션이라고 명명되어 있는 히치하이킹 행동을 예쁜꼬마선충의 특정 발생단계 즉 다우어 단계에서만 한다는 점에 착안하여 이 행동이 프로그램된 행동이라는 인식을 하게 된 것이었다. 행동은 근육의 작동으로 이루어지지만 거슬러 올라가 보면 신경세포가 환경을 인식하고 계산하고 의사결정을 하여 운동신경에 신호를 보내 근육이 움직이게 되는 과정을 포함한다. 즉 예쁜꼬마선충의 히치하이킹 행동을 연구하면 행동의 전반적인 과정에서 일어나는 가장 단순한 의사결정 기전을 이해하게 될 것이고 이런 현상이 고등동물에서도 적용될 수 있을 것으로 기대할 수 있다. 필자의 연구실에서는 지난 20년 동안 닉테이션 행동에 필요한 뉴런을 특정할 수 있었고, 닉테이션 빈도를 조절하는 유전자를 발견하였으며, 더 나아가서는 닉테이션을 하는 특별한 발생단계인 다우어의 커넥톰을 단일 시냅스 수준에서 완성하였다. 그 결과 다우어 시기 특이적인 시냅스들을 찾을 수 있었고 그 중 하나는 닉테이션에 중요한 역할을 한다는 것을 증명할 수 있었다. 히치하이킹 행동은 찰스 다윈이 자신의 저서 종의 기원에서 한 챕터를 할애하여 자세히 설명한 행동일 뿐 아니라 다윈의 별세 직전에 출판한 마지막 논문의 주제이기도 했다. 그런 중요성을 가지는 행동의 기전을 필자의 연구실에서 최초로 규명했으니 나름 스스로 자랑스러울 만하다 하겠다. 필자 연구실의 두 번째 연구업적은 텔로미어 유지 기전 관련 연구이다. 텔로미어는 진핵세포가 가지는 선형 염색체가 필연적으로 가질 수 밖에 없는 염색체 말단을 보호하는 핵산-단백질 복합체를 의미한다. 사람을 포함한 많은 생명체에서 텔로미어를 유지하기 위해서 텔로머레이즈 효소를 이용한다. 텔로머레이즈 효소를 발견한 과학자들이 2009년에 노벨상을 받은 것은 당연한 것이라 할 만하다. 그런데 텔로미어 유지에 텔로머레이즈만 관여하는 것이 아니라는 점이 떠오르게 된 것은 2000년 경이다. 호주의 리델 교수 연구실에서 사람의 암세포 중에서 텔로머레이즈 효소 작용이 다시 살아나 텔로미어 길이를 유지하는 경우가 대부분이기는 하지만 적지 않은 경우에 텔로머레이즈 없이 텔로미어를 유지하는, 그래서 대안적 텔로미어 유지기전이라고 부르게 되는, 새로운 현상을 발견하였다. 그 기전이 완벽하게 밝혀져 있지 않아서 필자의 연구실도 2004년부터 대안적 텔로미어 유지 기전에 대한 연구를 예쁜꼬마선충을 이용하여 시작하게 되었다. 약 9년 정도의 지난한 연구의 시행착오 끝에 예쁜꼬마선충에서도 대안적 텔로미어 기전이 작동하고 있음으로 규명하였고, 이러한 새로운 현상이 예쁜꼬마선충에서만 일어나는 현상이 아니라 생쥐 배아줄기 세포에서도 일어나고 있다는 점도 발견하게 되었다. 아직은 진행 중인 연구이지만 사람의 암세포에서도 이 새로운 유지기전이 존재할 것이라고 가정하고 탐색을 하고 있는 중이다. 아무도 설명하지 못했던 생명 현상에 대한 새로운 설명을 제시할 수 있는 것이 곧 새로운 발견이라고 믿는다. 필자의 연구실의 두 가지 예만 들었지만 이런 정도의 새로운 발견 연구는 이제 우리나라에서도 축적되고 있으니 머지않아 노벨상이 우리나라에도 주어질 것이라고 희망적으로 생각하게 된다. 학문후속세대들에게 꼭 남기고 싶은 말은, 생명과학의 최대의 매력은 하나를 알면 모르는 것이 더 많이 생긴다는 것이다. 아무것도 몰랐을 때는 무엇을 모르는지 몰라서 무엇을 질문해야 할지도 모르는 것이지만 조금씩 알아가면 새로운 질문이 떠오르고 그 다음에는 더 새롭게 깊은 질문이 꼬리를 물 것이다. 그럴 정도로 생명에 대해서는 우리가 모르는 것이 훨씬 많다. 호기심과 도전 정신으로 무장된 젊은이들이여, 생명과학의 현장으로 용감하게 나아 오라!!
7. 더 읽을 거리
본문에 있는 내용 중 깊이 있는 문제 제기와 해결 방법에 대한 공부를 하기 원하는 독자는 다음의 논문을 참고하시기 바란다. 그리고 질문이 생기면 elegans@snu.ac.kr로 연락 주시면 성심껏 답해 드릴 것을 약속한다.
- (2012) Nictation, a dispersal behavior of the nematode Caenorhabditis elegans, is regulated by IL2 neurons. Nat Neurosci.15(1):107-112.
- (2024) Comparative connectomics of dauer reveals developmental plasticity. Nat Commun. 15(1):1546. doi: 10.1038/s41467-024-45943-3.
- (2015) Telomere maintenance through recruitment of internal genomic regions. Nat Commun. 6:8189.
- (2021) Telomeres reforged with non-telomeric sequences in mouse embryonic stem cells. Nat Commun. 12(1):1097